FARADEY QANUNLARI – elektrolizin яsas qanunlarы; elektrokimyяvi reaksiyanыn getdiyi шяraitdя maddяnin saxlanmasыnыn цmumi qanununu яks etdirir. 1833–34 illяrdя M.Faradey tяrяfindяn kяшf edilmiшdir.
B i r i n c i q a n u n. Elektroliz prosesindя reaksiyaya girmiш електрод цзяриндя топланан maddяnin kцtlяsi (m) cяrяyan шiddяti (I ) vя elektrolizin mцddяti ilя (t) dцz mцtяnasibdir (Q=It) (fяrz edilir ki, I t-dяn asыlы deyil; яks halda kцtlя ![]() ilя mцtяnasibdir, burada t1 vя t2 – cяrяyanыn гошулма vя kяsilmя momentlяridir).
ilя mцtяnasibdir, burada t1 vя t2 – cяrяyanыn гошулма vя kяsilmя momentlяridir).
İ k i n c i q a n u n. Mцxtяlif elektrod proseslяrindя eyni miqdar elektrik yцkц keчяn zaman reaksiyaya girmiш maddяlяrin kцtlяlяrinin nisbяti onlarыn kimyяvi ekvivalentlяrи иля мцтанасибдир. F.q. bir tяnliklя ifadя olunur:
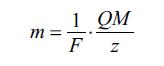
Burada M – elektrolizdя iшtirak edяn maddяnin mol. kцtlяsi; з – bu maddяnin bir molekulunun чevrilmяsinя uyьun olan elementar yцklяrin sayы; 1/F – bцtцn maddяlяr цчцn цmumi olan mцtяnasiblik яmsalы; F – Faradey sabiti, F=96484,56±0,27 Kl/mol. F.q.-nыn kimyяvi rabitяlяrin tяbiяtinin anlaшыlmasыnda vя atom-molekul nяzяriyyяsinin inkiшafыnda mцhцm rolu olmuшdur. Onlar 1-ci vя 2-ci nюv keчiricilяri ayыran sяrhяdlяrdя gedяn elektrokimyяvi чevrilmяlяri tяsvir edяn bцtцn tяnliklяrin чыxarыlmasыnda istifadя olunur. F.q. kulonometriyada vя cяrяyana gюrя reaksiyanыn чыxыmыnыn tяyin edilmяsindя tяtbiq edilir.















