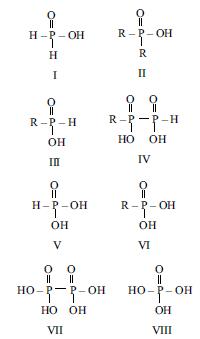
FOSFOR TURŞULARI – oksidlәşmә dәrәcәsi +1-dәn +5-әdәk olan fosforun oksigenli turşuları. XYP(O)OH quruluş vahidlәrindәn tәşkil olunmşdur; burada X vә Y – O, P, H vә ya üzvi radikaldır (bax Fosfor-üzvi birlәşmәlәr). Blazer vә Vormsa görә F.t.-nın formullarının qısa yazılışı (P1-turşu, P3-turşu vә s.; P atomu üzәrindәki indeks onun oksidlәşmә dәrәcәsini göstәrir) eynitәrkibli turşuların izomerlәrini fәrqlәndirmәyә imkan verir, mәs., H4P2O5 turşusunun izomerlәri P3 – O – P3 vә P2 – P4-turşularıdır. F.t.-na misal olaraq P1-turşuları – hipofosfit turşusu H3PO2 (formul1), fosfinat turşuları RR′P(O)OH (II), fosfonit turşuları RH2PO2 (III); P2– P2-turşusu – hipodifosfat turşusu H4P2O4 (IV); P3-turşuları – fosfit turşusu H3PO3 (V), fosfonat turşuları RP(O)(OH)2 (VI); P4– P4- turşu –hipofosfat turşusu H4P2O6 (VII); P5-turşusu – fosfat turşusunu (ortofosfat) H3PO4 (VIII) göstәrmәk olar.
Birәsaslı H3PO2, (HPO3)n; ikiәsaslı H4P2O5 (P3 –O – P3), H4P2O6 (P4 – P4); üçәsaslı H3PO4, H4P2O5, H4P2O6; dördәsaslı H4P2O7; beşәsaslı H5P3O8; altıәsaslı H6P6O12 [tsiklik vә ya (P3– P3)3c turşu] turşular kristal halında ayrılmışdır. Su ayırmaqla H3PO4-ün anion kondenslәşmәsindәn kondenslәşmiş turşular alınır; onların molekullarında öz aralarında ümumi oksigen atomu ilә birlәşmiş tetraedrik PO4 qrupu zәncirlәri (polifosfat turşuları), halqalar (metafosfat turşuları), şaxәli quruluşlar (ultrafosfat turşuları) әmәlә gәtirir.
H i p o f o s f i t t u r ş u s u H3PO2; tәr. 26,5°C, sıxlığı 1,49 q/sm3. Suda, etanolda, dietil efirindә yaxşı hәll olur. 50°C-dәn yuxarı temp-rda PH3, qırmızı P, H3PO4 vә H2-ә parçalanır; güclü reduksiyaedicidir. Qeyri-üzvi hipofosfit duzları, mәs., Na(H2PO2)·H2O әmәlә gәtirir. Hipofosfit turşusu hipofosfitlәrin H2SO4 vә ya oksalat turşusu ilә qarşılıqlı tәsirindәn, zәif turş sulu mühitdә PH3-ün oksidlәşmәsindәn alınır. Alkid qatranları
üçün antioksidant, poliamidlәr vә polivinilxlorid üçün işıq stabilizatorları, penopoliuretanlar alınmasında köpük stabilizatoru kimi istifadә edilir.
H i p o f o s f a t t u r ş u s u H4P2O6; tәr.70°C. Suda hәll olur. Mono- vә dihidratlar әmәlә gәtirir. 30°C-dәn yuxarı temp-rda qatı sulu mәhlullarda H3PO3 vә H3PO4-ә parcalanır. KMnO4 vә K2Cr2O7 ilә oksidlәşmәsindәn H3PO4 әmәlә gәlir. Hipofosfat turşusu vә ya P-un H3PO3 mәhlullarının hava ilә oksidlәşmәsindәn, P ilә xlorlu әhәngin qarşılıqlı tәsirindәn alınır. Qәlәvi metalların duzları suda yaxşı hәll olur, qәlәvi-torpaq vә ağır metalların duzları hәll olmur. Suda qızdırıldıqda hipofosfit vә fosfatlara qәdәr hidroliz olunur.
F o s f i t t u r ş u s u H3PO3; tәr. 73,6°C, sıxlığı 1,65 q/sm3. Suda yaxşı hәll olur. Suda qızdırıldıqda H2 ayrılmaqla H3PO4-ә qәdәr oksidlәşir; reduksiyaedicidir, Pt, Pd, Ag, Au vә s. Metalları onların duzlarının mәhlullarından çökdürür. PCl3-ün hidrolizindәn, P2O3-ün suda hәllolmasından vә ya H3PO3 duzlarının H2SO4 ilә qarşılıqlı tәsirindәn alınır. H3PO3-ün duzları olan fosfitlәr suda pis hәll olur (qәlәvi metalların duzlarından başqa), qızdırıldıqda ortofosfatlara vә oksidlәşmә dәrәcәsi aşağı olan P törәmәlәrinә parçalanır. H3PO3-ün metalların hidroksidlәrilә neytrallaşmasından fosfitlәr alınır ki, bunlar da qeyri-üzvi sintezdә reduksiyaedici, polivinilxloridin stabilizatoru (qurğuşun fosfit) kimi istifadә olunur.
P i r o f o s f a t t u r ş u s u H4P2O7; әrimә temp-rları 54,3°C vә 71,5°C olan iki polimorf modifikasiyada mövcuddur. Suda yaxşı hәll olur, mono-, penta- vә heksahidratlar әmәlә gәtirir. H3PO4-ün buxarlanmasından, P2O5 ilә H3PO4-ün qarşılıqlı
tәsirindәn, suda hәllolan pirofosfatlardan ion mübadilәsi ilә alınır. H4P2O7-nin duz- ları
pirofosfatlardır.
Əd.: Корбридж Д. Фосфор. Основы химии,
биохимии, технологии. Пер. с англ., M., 1982.















