HAL TƏNLİYİ – termodinamik tarazlıqda olan bircins sistemin tәzyiqi (p), hәcmi (V) vә temperaturu (T) arasında әlaqәni ifadә edәn tәnlik: f(p,V,T)= 0. Bu, sistemin U daxili enerjisini p, V, T, parametrlәrindәn ikisi ilә әlaqәlәndirәn kalorik H.t.-dәn fәrqli olaraq termik H. t. adlanır. Termik vә kalorik H. t. arasında әlaqә termodinamikanın ikinci qanunundan alınır: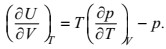 H t . termodinamika qanunlarının real maddәlәrә tәtbiq edilmәsinә imkan verir. O, yalnız termodinamika qanunlarının kömәyi ilә çıxarıla bilmәz, tәcrübәdәn tәyin edilir vә ya statistik fizikanın metodları ilә maddә quruluşu haqqındakı tәsәvvürlәr әsasında nәzәri olaraq hesablanır. İdeal qazın H. t. Klapeyron tәnliyidir: pv = RT (R – universal qaz sabiti, ν – bir mol qazın hәcmidir). Real qazların H. t. Van-der-Vaals tәnliyi
H t . termodinamika qanunlarının real maddәlәrә tәtbiq edilmәsinә imkan verir. O, yalnız termodinamika qanunlarının kömәyi ilә çıxarıla bilmәz, tәcrübәdәn tәyin edilir vә ya statistik fizikanın metodları ilә maddә quruluşu haqqındakı tәsәvvürlәr әsasında nәzәri olaraq hesablanır. İdeal qazın H. t. Klapeyron tәnliyidir: pv = RT (R – universal qaz sabiti, ν – bir mol qazın hәcmidir). Real qazların H. t. Van-der-Vaals tәnliyi 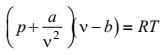 (a vә b molekullar arasındakı qarşılıqlı tәsiri vә onların hәcmini nәzәrә alan sabitlәr olub, qazın tәbiәtindәn asılıdır) vә virial tәnlikdir:
(a vә b molekullar arasındakı qarşılıqlı tәsiri vә onların hәcmini nәzәrә alan sabitlәr olub, qazın tәbiәtindәn asılıdır) vә virial tәnlikdir: 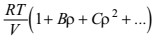 (ρ – qazın sıxlığı, B, C, vә s. 1-ci, 2-ci vә s. virial әmsallar adlanır, temp-rdan vә molekullar arasındakı qarşılıqlı tәsir qüvvәlәrindәn asılıdır). Bunlar nәzәri әsaslandırılmış tәnliklәrdir. Tarazlıq şüalanmasının H. t. Plank qanunu ilә ifadә olunur. Mayelәr üçün çoxlu sayda tәcrübi H. t. mövcuddur. Lakin nәzәri әsasları olan H. t. yoxdur. Bәrk cisimlәrin H. t. elastiklik modulunun temp-r vә tәzyiqdәn asılılığını göstәrir.
(ρ – qazın sıxlığı, B, C, vә s. 1-ci, 2-ci vә s. virial әmsallar adlanır, temp-rdan vә molekullar arasındakı qarşılıqlı tәsir qüvvәlәrindәn asılıdır). Bunlar nәzәri әsaslandırılmış tәnliklәrdir. Tarazlıq şüalanmasının H. t. Plank qanunu ilә ifadә olunur. Mayelәr üçün çoxlu sayda tәcrübi H. t. mövcuddur. Lakin nәzәri әsasları olan H. t. yoxdur. Bәrk cisimlәrin H. t. elastiklik modulunun temp-r vә tәzyiqdәn asılılığını göstәrir.
“Azərbaycan” xüsusi cildi (Az)“Azərbaycan” xüsusi cildi (rus)I CİLDII CİLDIII CİLDIV CİLDV CİLDVI CİLDVII CİLDVIII CİLDIX CİLDX CİLDXI CİLD

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, “Azərbaycan” xüsusi cildi (Azərbaycan dilində) |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | 2007 |
| ISBN: | 978-9952-441-01-7 |
| Səhifələrin sayı: | 881 |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, “Azərbaycan” xüsusi cildi (rus dilində) |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | 2012 |
| ISBN: | 978-9952-441-01-7 |
| Səhifələrin sayı: | 881 |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, I CİLD |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | 2009 |
| ISBN: | 978-9952-441-02-4 |
| Səhifələrin sayı: | 608 |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, II CİLD |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | 2010 |
| ISBN: | 978-9952-441-05-5 |
| Səhifələrin sayı: | 604 |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, III CİLD |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | 2011 |
| ISBN: | 978-9952-441-07-9 |
| Səhifələrin sayı: | 604 |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, IV CİLD |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | 2013 |
| ISBN: | 978-9952-441-03-1 |
| Səhifələrin sayı: | 608 |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, V CİLD |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | 2014 |
| ISBN: | 978-9952-441-10-9 |
| Səhifələrin sayı: | 592 |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, VI CİLD |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | 2015 |
| ISBN: | 978-9952-441-11-6 |
| Səhifələrin sayı: | 608 |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, VII CİLD |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | 2016 |
| ISBN: | 978-9952-441-12-3 |
| Səhifələrin sayı: | 608 |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, VIII CİLD |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | |
| ISBN: | |
| Səhifələrin sayı: |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, IX CİLD |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | 2019 |
| ISBN: | 978-9952-441-17-8 |
| Səhifələrin sayı: | 600 |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, X CİLD |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili | 2020 |
| ISBN: | 978-9952-441-18-5 |
| Səhifələrin sayı: | 600 |

| Sərlövhə: | Azərbaycan Milli Ensiklopediyası, XI CİLD |
| Nəşriyyat: | "Azərbaycan Milli Ensiklopediyası" Elmi Mərkəzi |
| Nəşr yeri: | Bakı |
| Nəşr ili: | 2024 |
| ISBN: | 978-9952-441-20-8 |
| Səhifələrin sayı: | 600 |
GİYAN – HİDROKREKİNQ
HAL TƏNLİYİ
HAL TƏNLİYİ – termodinamik tarazlıqda olan bircins sistemin tәzyiqi (p), hәcmi (V) vә temperaturu (T) arasında әlaqәni ifadә edәn tәnlik: f(p,V,T)= 0. Bu, sistemin U daxili enerjisini p, V, T, parametrlәrindәn ikisi ilә әlaqәlәndirәn kalorik H.t.-dәn fәrqli olaraq termik H. t. adlanır. Termik vә kalorik H. t. arasında әlaqә termodinamikanın ikinci qanunundan alınır: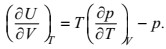 H t . termodinamika qanunlarının real maddәlәrә tәtbiq edilmәsinә imkan verir. O, yalnız termodinamika qanunlarının kömәyi ilә çıxarıla bilmәz, tәcrübәdәn tәyin edilir vә ya statistik fizikanın metodları ilә maddә quruluşu haqqındakı tәsәvvürlәr әsasında nәzәri olaraq hesablanır. İdeal qazın H. t. Klapeyron tәnliyidir: pv = RT (R – universal qaz sabiti, ν – bir mol qazın hәcmidir). Real qazların H. t. Van-der-Vaals tәnliyi
H t . termodinamika qanunlarının real maddәlәrә tәtbiq edilmәsinә imkan verir. O, yalnız termodinamika qanunlarının kömәyi ilә çıxarıla bilmәz, tәcrübәdәn tәyin edilir vә ya statistik fizikanın metodları ilә maddә quruluşu haqqındakı tәsәvvürlәr әsasında nәzәri olaraq hesablanır. İdeal qazın H. t. Klapeyron tәnliyidir: pv = RT (R – universal qaz sabiti, ν – bir mol qazın hәcmidir). Real qazların H. t. Van-der-Vaals tәnliyi 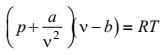 (a vә b molekullar arasındakı qarşılıqlı tәsiri vә onların hәcmini nәzәrә alan sabitlәr olub, qazın tәbiәtindәn asılıdır) vә virial tәnlikdir:
(a vә b molekullar arasındakı qarşılıqlı tәsiri vә onların hәcmini nәzәrә alan sabitlәr olub, qazın tәbiәtindәn asılıdır) vә virial tәnlikdir: 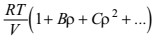 (ρ – qazın sıxlığı, B, C, vә s. 1-ci, 2-ci vә s. virial әmsallar adlanır, temp-rdan vә molekullar arasındakı qarşılıqlı tәsir qüvvәlәrindәn asılıdır). Bunlar nәzәri әsaslandırılmış tәnliklәrdir. Tarazlıq şüalanmasının H. t. Plank qanunu ilә ifadә olunur. Mayelәr üçün çoxlu sayda tәcrübi H. t. mövcuddur. Lakin nәzәri әsasları olan H. t. yoxdur. Bәrk cisimlәrin H. t. elastiklik modulunun temp-r vә tәzyiqdәn asılılığını göstәrir.
(ρ – qazın sıxlığı, B, C, vә s. 1-ci, 2-ci vә s. virial әmsallar adlanır, temp-rdan vә molekullar arasındakı qarşılıqlı tәsir qüvvәlәrindәn asılıdır). Bunlar nәzәri әsaslandırılmış tәnliklәrdir. Tarazlıq şüalanmasının H. t. Plank qanunu ilә ifadә olunur. Mayelәr üçün çoxlu sayda tәcrübi H. t. mövcuddur. Lakin nәzәri әsasları olan H. t. yoxdur. Bәrk cisimlәrin H. t. elastiklik modulunun temp-r vә tәzyiqdәn asılılığını göstәrir.
HAL TƏNLİYİ
HAL TƏNLİYİ – termodinamik tarazlıqda olan bircins sistemin tәzyiqi (p), hәcmi (V) vә temperaturu (T) arasında әlaqәni ifadә edәn tәnlik: f(p,V,T)= 0. Bu, sistemin U daxili enerjisini p, V, T, parametrlәrindәn ikisi ilә әlaqәlәndirәn kalorik H.t.-dәn fәrqli olaraq termik H. t. adlanır. Termik vә kalorik H. t. arasında әlaqә termodinamikanın ikinci qanunundan alınır: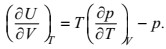 H t . termodinamika qanunlarının real maddәlәrә tәtbiq edilmәsinә imkan verir. O, yalnız termodinamika qanunlarının kömәyi ilә çıxarıla bilmәz, tәcrübәdәn tәyin edilir vә ya statistik fizikanın metodları ilә maddә quruluşu haqqındakı tәsәvvürlәr әsasında nәzәri olaraq hesablanır. İdeal qazın H. t. Klapeyron tәnliyidir: pv = RT (R – universal qaz sabiti, ν – bir mol qazın hәcmidir). Real qazların H. t. Van-der-Vaals tәnliyi
H t . termodinamika qanunlarının real maddәlәrә tәtbiq edilmәsinә imkan verir. O, yalnız termodinamika qanunlarının kömәyi ilә çıxarıla bilmәz, tәcrübәdәn tәyin edilir vә ya statistik fizikanın metodları ilә maddә quruluşu haqqındakı tәsәvvürlәr әsasında nәzәri olaraq hesablanır. İdeal qazın H. t. Klapeyron tәnliyidir: pv = RT (R – universal qaz sabiti, ν – bir mol qazın hәcmidir). Real qazların H. t. Van-der-Vaals tәnliyi 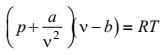 (a vә b molekullar arasındakı qarşılıqlı tәsiri vә onların hәcmini nәzәrә alan sabitlәr olub, qazın tәbiәtindәn asılıdır) vә virial tәnlikdir:
(a vә b molekullar arasındakı qarşılıqlı tәsiri vә onların hәcmini nәzәrә alan sabitlәr olub, qazın tәbiәtindәn asılıdır) vә virial tәnlikdir: 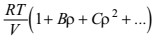 (ρ – qazın sıxlığı, B, C, vә s. 1-ci, 2-ci vә s. virial әmsallar adlanır, temp-rdan vә molekullar arasındakı qarşılıqlı tәsir qüvvәlәrindәn asılıdır). Bunlar nәzәri әsaslandırılmış tәnliklәrdir. Tarazlıq şüalanmasının H. t. Plank qanunu ilә ifadә olunur. Mayelәr üçün çoxlu sayda tәcrübi H. t. mövcuddur. Lakin nәzәri әsasları olan H. t. yoxdur. Bәrk cisimlәrin H. t. elastiklik modulunun temp-r vә tәzyiqdәn asılılığını göstәrir.
(ρ – qazın sıxlığı, B, C, vә s. 1-ci, 2-ci vә s. virial әmsallar adlanır, temp-rdan vә molekullar arasındakı qarşılıqlı tәsir qüvvәlәrindәn asılıdır). Bunlar nәzәri әsaslandırılmış tәnliklәrdir. Tarazlıq şüalanmasının H. t. Plank qanunu ilә ifadә olunur. Mayelәr üçün çoxlu sayda tәcrübi H. t. mövcuddur. Lakin nәzәri әsasları olan H. t. yoxdur. Bәrk cisimlәrin H. t. elastiklik modulunun temp-r vә tәzyiqdәn asılılığını göstәrir.










